Configuración electrónica
En física y química, la configuración electrónica es la manera en la cual los electrones se estructuran o se modifican en un átomo, molécula o en otra estructura físico-química, de acuerdo con el modelo de capas electrónico, en el cual las funciones de ondas del sistema se expresa como un producto de orbitales antisimetrizadas.1 2 Cualquier conjunto de electrones en un mismo estado cuántico deben cumplir el principio de exclusión de Pauli. Por ser fermiones (partículas de espín semientero) el principio de exclusión de Pauli nos dice que esto es función de onda total (conjunto de electrones) debe ser antisimétrica.3 Por lo tanto, en el momento en que un estado cuántico es ocupado por un electrón, el siguiente electrón debe ocupar un estado cuántico diferente.Valores de los números cuánticos
En el caso de los orbitales de los átomos hidrogenoides el número cuántico principal n está asociado a los diferentes niveles de energía orbital permitidos o niveles cuánticos; los valores que toma son 1, 2, 3, 4, 5,... Para n=1 se tiene el nivel de menor energía. Todos los estados con el mismo número cuántico principal forman una capa (o nivel). Por razones históricas, estas capas electrónicas (por ejemplo en espectroscopia de rayos X) también se denotan como K, L, M, N,... El segundo número cuántico l corresponde al momento angular del estado. Estos estados tienen la forma de armónicos esféricos, y por lo tanto se describen usando polinomios de Legendre. También por razones históricas a estas subcapas (o subniveles), se les asigna una letra, que hace referencia al tipo de orbital que describe el estado electrónico (s, p, d, f, ...),Los valores que puede tomar l son: 0, 1, 2, 3, 4,...,(n-1), siendo n el número cuántico principal. El tercer número cuántico, m, puede tomar los valores desde -l a l, y por lo tanto hay un total de 2l+1 estados degenerados posibles. Cada uno de éstos puede ser ocupado por dos electrones con espines opuestos, consecuencia de los dos posibles valores de la proyección sobre el eje z del espín electrónico, ms, que puede tomar los valores +1/2 ó -1/2. Esto da un total de 2(2l+1) electrones en total (tal como se puede ver en la tabla siguiente).| Valor de l | Letra | Máximo número de electrones |
|---|---|---|
| 0 | s | 2 |
| 1 | p | 6 |
| 2 | d | 10 |
| 3 | f | 14 |
| Número cuántico | Valores posibles | |
| n | 1, 2, 3,... | |
| l | 0,..., (n-1) | |
| m | -l, (-l+1),..., 0,....,(+l-1), +l | |
| ms | -1/2, +1/2 |
Notación
Para átomos con muchos electrones, esta notación puede ser muy larga por lo que se utiliza una notación abreviada, que tiene en cuenta que las primeras subcapas son iguales a las de algún gas noble. Por ejemplo, el fósforo, difiere del argón y neón (1s2 2s2 2p6) únicamente por la presencia de la tercera capa. Así, la configuración electrónica del fósforo se puede escribir respecto de la del neón como: [Ne] 3s2 3p3. Esta notación es útil si tenemos en cuenta que la mayor parte de las propiedades químicas de los elementos vienen determinadas por las capas más externas.El orden en el que se escriben los orbitales viene dado por la estabilidad relativa de los orbitales, escribiéndose primero aquellos que tienen menor energía orbital. Esto significa que, aunque sigue unas pautas generales, se pueden producir excepciones. La mayor parte de los átomos siguen el orden dado por la regla de Madelung. Así, de acuerdo con esta regla, la configuración electrónica del hierro se escribe como: [Ar] 4s2 3d6. Otra posible notación agrupa primero los orbitales con el mismo número cuántico n, de tal manera que la configuración del hierro se expresa como [Ar] 3d6 4s2 (agrupando el orbital 3d con los 3s y 3p que están implicitos en la configuración del argón).
El superíndice 1 de los orbitales ocupados por un único electrón no es obligatorio.4 Es bastante común ver las letras de los orbitales escritas en letra itálica o cursiva. Sin embargo, la Unión Internacional de Química Pura y Aplicada (IUPAC) recomienda utilizar letra normal, tal y como se realiza aquí.
Distribución electrónica
Es la distribución de los electrones en los subniveles y orbitales de un átomo. La configuración electrónica de los elementos se rige según el diagrama de Moeller:Para comprender el diagrama de Moeller se utiliza la siguiente tabla:
| s | p | d | f | |
|---|---|---|---|---|
|
|
|
|||
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- sólo se pueden ocupar los orbitales con un máximo de dos electrones, en orden creciente de energía orbital: los orbitales de menor energía se llenan antes que los de mayor energía.
| s | p | d | f | |
|---|---|---|---|---|
|
|
|
|||
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Para determinar la configuración electrónica de un elemento, basta con calcular cuántos electrones hay que acomodar y entonces distribuirlos en los subniveles empezando por los de menor energía e ir llenando hasta que todos los electrones estén distribuidos. Un elemento con número atómico mayor tiene un electrón más que el elemento que lo precede. El subnivel de energía aumenta de esta manera:
- Subnivel s, p, d o f: Aumenta el nivel de energía.
Orbital o REEMPE
En química se usa la expresión REEMPE para designar el valor esperado de un operador densidad de estados de dos electrones con .
En otras palabras: la región donde existe mayor posibilidad de
encontrar como máximo 2 electrones que se mueven en forma paralela y en
sentidos contrarios. Su nombre proviene de Región de Espacio Energético de Manifestación Probabilística del Electrón.
.
En otras palabras: la región donde existe mayor posibilidad de
encontrar como máximo 2 electrones que se mueven en forma paralela y en
sentidos contrarios. Su nombre proviene de Región de Espacio Energético de Manifestación Probabilística del Electrón.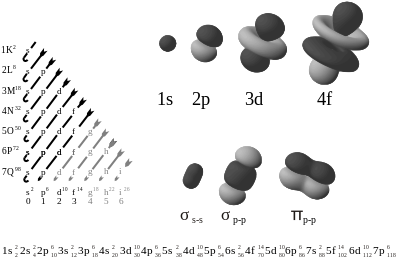
No hay comentarios:
Publicar un comentario